Piszkos drogok az immunrendszerben
További Tech-Tudomány cikkek
A hasmenéssel járó megbetegedések 70-80 százalékát vírusfertőzés okozza, amely ellen az antibiotikumok hatástalanok. Ezzel szemben világszerte a betegek 40 százalékát (sőt egyes területeken a 80 százalékát) antibiotikumokkal próbálják kezelni. E hatóanyagok szükségtelen túlhasználata (illetve az előírt kúra idő előtti félbehagyása) a fő oka a rezisztens baktériumtörzsek aggasztó terjedésének. Ebben persze semmi meglepő nincs, hiszen csak az evolúciót látjuk munka közben. A véletlenül létrejövő mutációk némelyike ellenálló képességgel ruházza fel a mikrobát az antibiotikummal szemben, így ő előnybe kerül társaihoz viszonyítva, és terjedni kezd a populációban. Ez óhatatlan folyamat, de az ésszerűtlen viselkedéssel sokszorosára gyorsíthatjuk.
Pedig a kórokozók maguktól is rendkívül talpraesettek, ha a rezisztenciagének elterjesztéséről van szó.
A baktériumok rendkívül piszkos trükköt vetnek be: egymás között cserélgetnek géneket Így egészen távoli fajok is készen kapják az ellenálló képességet. Néha ezek a baktériumok olyan távoli rokonok, mint a muslica és mi
– mondja Pál Csaba, az MTA SZBK tudományos főmunkatársa.
Tehát nem kell minden baktériumfajnak külön-külön felfedeznie az antibiotikum ellen hatásos rezisztencia mikéntjét. Elég, ha vírusok, vagy rövid örökítőanyag-szakaszok (plazmidok) segítségével megszerzi a másiktól. E mechanizmus (a horizontális géntranszfer) nem új, évmilliók óta így megy, de segítségével a baktériumok rendkívül hatékonyan képesek reagálni a változó környezet kihívásaira.
A géntranszfer által a genetikai vívmányok szédítően nagy sebességgel terjedhetnek. Miután egy antibiotikum-rezisztencia gént detektálnak Indiában, öt évvel később már az összes földrészen izolálható. Tehát nem maga a baktérium terjed feltétlenül, csak az ellenálló képességet biztosító genetikai elem. Így
egy biológiai innováció a legkülönfélébb betegségek kórokozóit is sokkal veszélyesebbé teheti.
E félelmetesen ütőképes mechanizmust látva az a csoda, hogy az állandóan velünk élő (bőrünkön és beleinkben található) baktériumok nem ölnek meg minket azonnal. Mert bár jelentős részük úgynevezett barátságos mikroba, azért szép számmal vannak kevésbé barátságosak is, amelyek kordában tartás nélkül szíves örömest megbetegíthetnének minket. Látszólag minden körülmény adott e bélbaktériumok számára, hogy rezisztenssé váljanak a szervezet által termelt, néhány aminosavból álló (peptid típusú) antimikrobiális hatású anyagokkal szemben. Hiszen rengetegen vannak, és e rövid fehérjeláncok folyamatosan érik őket, így rengeteg alkalmuk lehet, hogy kifejlesszék az ellenálló képességet. Ez mégsem történik meg, és ez reményt nyújthat az azokkal a kórokozókkal szembeni küzdelemben is, amelyek az elérhető szintetikus antibiotikumok többségére már csak leereszkedő félmosollyal legyintenek.
„Az antimikrobiális peptidek természetes immunrendszerünk részei. A káros baktériumokkal szembeni első védelmi vonalat jelentik ők - így Pál Csaba. - A hasznos bélbaktériumaink rezisztensek ezekkel szemben, és ez nagyon jó. Felmerül viszont a kérdés, hogy a baráti bélbaktériumok átadhatják-e a peptidrezisztencia-géneket a káros mikrobáknak.”
De úgy tűnik, a rezisztencia így nem adódhat át.
Az új kórokozó baktériumok, hiába kerülnek az ellenálló mikrobák közelébe, nem képesek átvenni tőlük ezt a képességet. Az immunrendszerünk láthatóan felfedezte azokat a mechanizmusokat, amelyekkel megkerülheti a horizontális géntranszfer támasztotta veszélyeket. Sajnos e mechanizmus hatékonysága korlátozott, nem működik minden kórokozó ellen, de alapvető törvényszerűségeit talán fel lehet használni az új típusú antibiotikumok fejlesztése során.
A Nature Microbiologyban megjelent tanulmány szerint a peptidek ütőképességét az biztosítja, hogy komplex módon hatnak a kórokozókra. Több ponton egyszerre támadják, például ugyanaz a molekula egyszerre bontja a baktérium sejtfalát, és kapcsolódik a DNS-éhez, meggátolva annak lemásolását. Ezek hiába egyetlen peptid hatásai, ellenük csak külön-külön kifejlődött mechanizmusokkal lehet védekezni, e készségek pedig külön-külön géneket igényelnek.
Piszkos drogoknak is hívják e hatásuk miatt ezeket a peptideket, hiszen a kórokozó szempontjából rendkívül álnok módon hatnak
– mondja a kutató. Az antimikrobiális peptidek egyes hatásai ellen védelmet biztosító gének önmagukban semmit sem érnek, mert a másik hatás ugyanúgy elpusztítja a baktériumot. A géntranszferrel pedig szinte kizárt, hogy az összes gén egyszerre átkerüljön a kórokozóba.
Collateral damage
Pál Csabáék kutatócsoportjának eredményei már korábban is a nemzetközi tudományos reflektorfénybe kerültek. Kimutatták egy, a multidrog-rezisztenciával épp ellentétes hatású jelenség, az úgynevezett kollaterális szenzitizáció jelentőségét, olvasható az MTA honlapján. Az elmúlt évek keserű tapasztalatai révén közismertté vált, hogy a baktériumok, miután ellenálló képességet szereztek egy antibiotikum ellen, nagyon gyakran más hatóanyagokkal szemben is ellenállóvá válnak - ez a keresztrezisztencia. Sokkal kevésbé ismert, hogy ennek fordítottja is lejátszódhat.
„A kollaterális szenzitizálás során a rezisztens baktérium hiperérzékennyé válik válik egy vagy több másik antibiotikumra” – mondja Pál Csaba. Valószínűleg a rezisztenciagéneknek van ilyen – a baktérium szempontjából – előnytelen mellékhatásuk. Például előfordul, hogy az ellenálló képesség alapja, hogy az egyik antibiotikum számára átjárhatatlanná válik a sejtmembrán. Viszont ezzel párhuzamosan éppen megnő az áteresztő képessége a másik hatóanyag szempontjából.
Kérdés viszont, hogy e jelenség mennyire gyakori, hiszen míg e mechanizmus a tudományos körökön kívül szinte ismeretlen, addig minden a multidrog-rezisztenciáról szól. Pál Csaba szerint a laboratóriumban gyakran előfordul e szenzitizáció, és megvan rá az esély, hogy a klinikumban is kiaknázható lesz a jövőben. Ha olyan antibiotikum-koktélokkal kezelnék a betegeket, amelyek egymás ellen kölcsönösen szenzitizációt kiváltó antibiotikumokat tartalmaznak, akkor elméletileg sokkal ütőképesebb gyógyszerkeverékeket lehetne létrehozni.
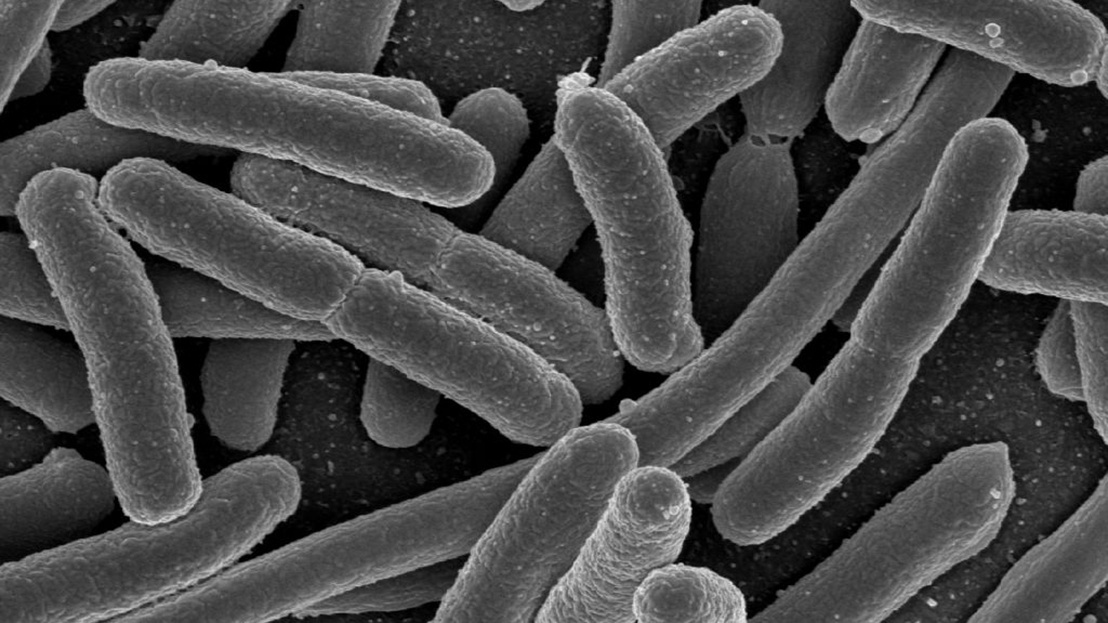
(Borítókép: A bélflórában természetes módon megtalálható Escherichia coli baktérium elektronmikroszkópos képe - forrás: National Institutes of Health / Wikimedia Commons)