Magyar kutatók csináltak Robotzsarut az egerekből

További Tech-Tudomány cikkek
Az ember és a főemlősök látása alapvetően két részből tevődik össze. A látóterünk közepén élesen látunk, ezt a retina sárgafolt (makula) nevű területére vetülő fény teszi lehetővé. A sárgafoltban nagyon sűrűn állnak a fényérzékelő csapok, más sejtek sokkal ritkábban vannak közöttük, ennek köszönhetően a retinának ezen a kicsiny területén nagyon éles a látásunk. A látótér szélei felé elmosódottan érzékeljük a fényt, ez a perifériás látás.
Örökletes vagy idős korban fellépő betegségeknél az éleslátás és a perifériás látás is romolhat. Előbbit okozza a makuladegeneráció, amely szörnyen frusztáló betegség, hiszen bárhová néz az ember, mindig épp középen nem fog látni rendesen, miközben a periférián úgy-ahogy, de lát valamennyit. Ritkábban az is előfordul, hogy a látótér szélétől terjed befelé a fokozatos megvakulás, így a teljes vakság előtt egy fajta csőlátással kénytelen együtt élni az ember.
A degenerálódó opszin
A retinában lévő fényérzékelő fotoreceptor sejtek (az ún. csapok és a pálcikák) egy opszin nevű fehérje révén alakítják a fényt elektromos ingerületté, amit a retina sejtáramkörei dolgoznak fel, és küldenek a látóidegen keresztül az agyba. A degeneratív szembetegségek legtöbbször a fotoreceptorok molekuláris folyamatait megzavaró mutációk miatt alakulnak ki. A degeneráció során a receptorok fényérzékelő nyúlványa tűnik el először, azonban a sejttest még egy ideig képes továbbélni.
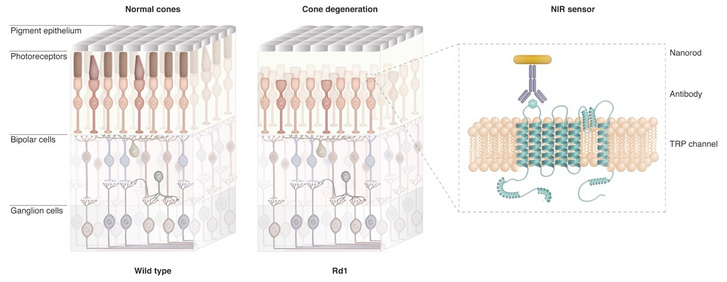
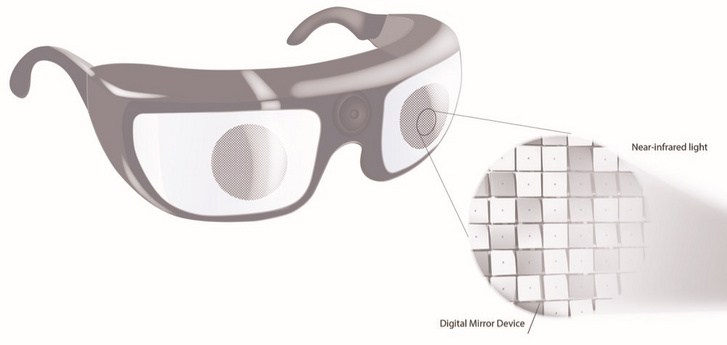
Ilyen esetekben megoldást kínálhat az, ha génterápás úton más fényérzékeny fehérjét kódoló génszekvenciát juttatnak a sejtekbe. Ilyen, úgynevezett optogenetikus fehérjék alkalmazásával erős kék fény hatására a degenerálódó sejtek újra ingerelhetővé válnak. A látásfunkciók visszaállításához a betegre egy a külvilág képét az optogenetikai fehérje hullámhosszára átalakító bionikus szemüveget erősítenek. A világon több helyen, így a Pázmány Egyetemen is fejlesztenek bionikus szemüveget.
Az optogenetikai fehérjék különféle mikroorganizmusokból nyerhetők ki, a génjeiket hosszú évek óta tökéletesítik, és alkalmazzák őket az élettudomány számos területén. Segítségükkel képesek vagyunk az idegsejtek működését igényeinknek megfelelően befolyásolni (például gerjeszteni vagy gátolni lehet így a neuronokat). A fehérjéket úgy lehet ki vagy bekapcsolni, ha megvilágítjuk őket a megfelelő hullámhosszú fénnyel. Ha tehát bevisszük a retina receptoraiba egy optogenetikai fehérje génjét, akkor a sejt termelni fogja a fénnyel aktiválható fehérjét, s ezáltal pótolhatjuk az elvesztett opszin fehérje funkcióját
- mondta el az Indexnek Hillier Dániel, a Természettudományi Kutatóközpont Vizuális rendszerek neurobiológiája csoport vezetője és a Pázmány Egyetem Információs Technológiai és Bionikai Karának oktatója, aki részt vett a Bázeli Molekuláris és Klinikai Szemészeti Kutatóintézet kutatásában.
Infravörös jövő
A ma alkalmazott optogenetikai fehérjék a látható fényre érzékenyek. Azonban e fehérjék aktiválásához olyan erős megvilágításra van szükség, ami elvakítja a páciens még működő fotoreceptorait. Ironikus módon épp az a tény köti meg a kutatók kezét, hogy a látóterük egy részén megvakult emberek bizonyos fokú látással még rendelkeznek. Így etikailag nem megengedhető, hogy olyan beavatkozásoknak vessék alá őket, amely ugyan képes lehet valamilyen csökkent látásélményt visszaadni nekik, de ennek az az ára, hogy a megmaradt természetes látásuktól esetleg megfosztják őket.
Emiatt született az az ötlet a bázeli kutatóintézet Roska Botond által vezetett kutatócsoportjában, hogy tegyék a látható fény tartományán kívül eső hullámhosszú fényre érzékennyé a degenerálódó fotoreceptorokat. Az ötlet szerint tehát a mesterséges látás hullámhossz-tartományát el kell választani a természetes látástól, hogy a kettő ne zavarja egymást. Ha megmarad ugyanis a természetes látás egy része, a beteg agya esetleg képes lesz a természetes és a mesterséges információt együttesen értékelni, és így még teljesebb látásélményhez juthat.
Ahogy a látható fénnyel aktiválható optogenetikai fehérjéket is a természetben találták meg, így ennek az ötletnek a megvalósításakor is olyan fajokat kerestek, melyek képesek a látható tartományon túli fénysugarak érzékelésére. A célnak megfelelnek
egyes denevérek és kígyófajok, amelyek képesek áldozataik által leadott infravörös sugárzás érzékelésére, és ezáltal tudják a prédát pontosabban lokalizálni.
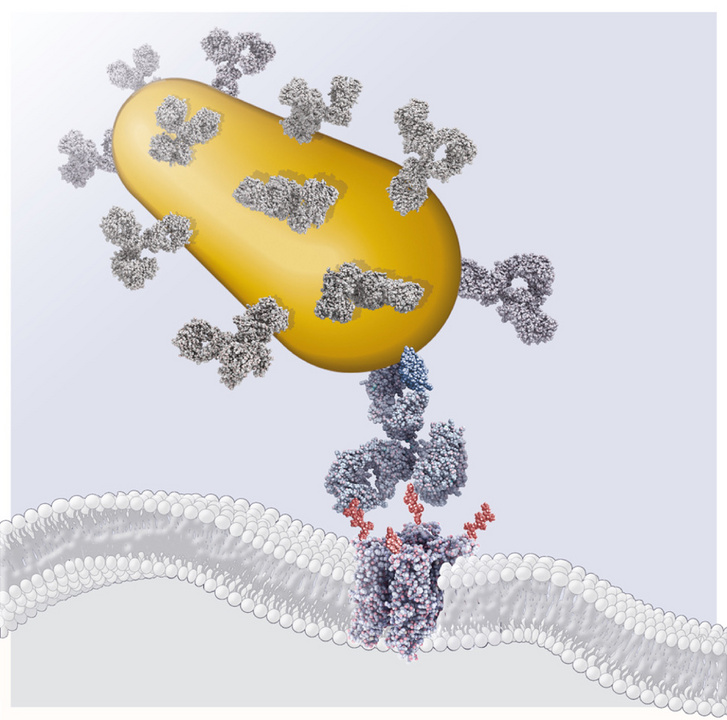
A kidolgozott rendszer központi eleme az infravörös fényre, azaz hőre érzékeny fehérje génje. Csupán ezt a fehérjét bejuttatva azonban még nem lehetett elég erősen aktiválni a fotoreceptorokat, mert a megfelelő aktivációhoz olyan erős hőt kellett volna sugározni, hogy az praktikusan megsütötte volna a retinát. Érzékenyebbé kellett tenni hát a fehérjéket. Ehhez nehezen lehetett volna stílusosabb eszközöket találni az arany nanopálcikáknál.
Arany antennák, mi más?
A nanopálcikákat, egy antennához hasonlóan, a bionikus szemüveg által vetített infravörös hullámhosszra hangolták, így a sugárzást hő formájában közvetlen környezetükben adják le. A harmadik komponens egy olyan antitest, amely azt biztosítja, hogy a nanorudak a fotoreceptorba bevitt hőérzékeny fehérjékhez kapcsolódjanak. A három elem együttesen biztosítja, hogy a besugárzott infravörös fény nagyon hatékonyan a hőre érzékenyített fotoreceptorokat ingereje, és ne jusson felesleges hő a retina más részeire.
A módszer emberi terápiára való alkalmazhatóságát két fontos kísérlettel mutatták meg. A látókéreg az emberben a tudatos látás kapuja, ezért vak egerekben bizonyították, hogy az infravörös fény által kiváltott aktivitás a látókéreg sejtjeit is aktiválja (vagyis eljut az információ az agyba).
A másik fontos kísérlet alapját a Semmelweis Egyetem Szabó Arnold által vezetett csoportja által fejlesztett, az emberi retina életben tartását ehetővé tévő módszer adta. A kutatók kimutatták, hogy az optogenetikai fehérjével, és a hozzájuk antitesteken kapcsolt arany nanorudakkal kezelt
vak emberi retina ganglionsejtjeit is hatékonyan képes aktiválni az infravörös hullámhosszú fényinger.
Az a jövő kérdése, hogy ez a kezelés mennyire tudja helyreállítani a látást. A bionikus szemüvegek jelenlegi fejlettségi szintjén még nem lehet ugyanolyan részletgazdagságú képet vetíteni a retinára. De a megoldás elméletileg nem lehetetlen.
(Borítókép: Index)




