Célzott rákgyógyítás magyar kutatótól
További Tudomány cikkek
-
 Magyar fejlesztés forradalmasíthatja a napelemparkok telepítését
Magyar fejlesztés forradalmasíthatja a napelemparkok telepítését - Eddig ismeretlen fajokat és hegyeket is találtak a víz alatt és a víz fölött is
- Van, aki még a szekrény hátuljában árválkodó bögrét is megsajnálja
- Olyan meleg az összes óceán, hogy kifehérednek a korallok
- Kiderült az igazság a Pfizer- és Moderna-vakcinákról
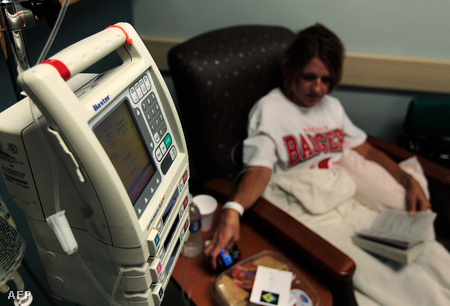
Dr. Dohán Orsolya belgyógyász, endokrinológus, klinikai onkológus 2000 óta doglozik együtt egy amerikai rákkutató csoporttal. Azóta számos neves külföldi szakfolyóiratban jelentek meg cikkei, a legutóbbi éppen a Proceedings of the National Academy of Sciencesben (PNAS). Az ott bemutatott kutatás egy lépéssel ismét közelebb vitte a tudományt a rákgyógyítással kapcsolatos problémák megoldásához.
Ágyúval verébre
A rák kezelésére jelenleg három bevett, ám közel sem tökéletes módszer létezik. A gyógyítás kemoterápiával, radioterápiával és/vagy radikális sebészi műtéttel történik. Vannak azonban olyan daganattípusok, amelyeket műtéti úton nem lehet eltávolítani, ezeknél csak a kemo-, vagy a radioterápia jöhet szóba.

A radioterápia úgy működik, hogy nagy energiájú sugárzással károsítják a daganat sejtjeinek DNS- ét, így gátolva a tumorsejtek osztódását, és kiváltva azok pusztulását. Ez a kezelés nem szelektív, így mind az ép, mind a daganatos sejtekre hat, mivel azonban a tumorokban nagyobb a sejtosztódás üteme, azaz nagyobb az osztódásra készülő, vagy az épp osztódásban lévő sejtek száma, a daganatoknak nagyobb a sugárérzékenységük.
A kemoterápia során különféle gyógyszerekkel gátolják a rákos sejtek osztódását, ezáltal a tumor növekedését. Ez a módszer azonban sok, nem kívánt mellékhatással jár, mivel az alkalmazott szerek nem elég specifikusak, az elpusztítandó daganaton kívül károsítják a szervezet ép sejtjeit is.
Célzott támadás
Dohán Orsolya a New York-i Albert Einstein Egyetem Nacy Carrasco által vezetett kutatócsoportjával együtt ezzel szemben egy olyan, daganatot elpusztító megoldáson dolgozik, amelynek alkalmazásakor nem kell az egész szervezetet radioterápiás eljárásnak kitenni.
Emellett módszerük hatalmas előnye, hogy nemcsak lassítja, vagy ideiglenesen megállítja a rákos daganatok kifejlődését, illetve továbbterjedését, hanem képes azt teljes mértékben elpusztítani.
Ennek eléréséhez a natrium-jodid-szinportert (NIS, natrium iodide symporter) használják fel. A NIS egy úgynevezett transzportfehérje, amely a jódtartalmú pajzsmirigyhormonok termelésében tölt be élettani szerepet. A vérből natriumionok segítségével jodidiont pumpál a sejtekbe, így koncentrálja a hormontermelésben fontos szerepet játszó jódot a pajzsmirigyben.
Régi ismerős, új szerepben
A NIS fehérje működését már mintegy 60 éve használja az orvostudomány a pajzsmirigydaganat gyógyítására. Ehhez a jód beta sugárzó izotópját használják (131-I), amelyet a NIS felhalmoz a pajzsmirigydaganatban, és az így keletkező lokális sugárzással a daganatszövetet elpusztítja. A pajzsmirigydaganatok radiojódterápiája eddig a legsikeresebb, rutinszerűen alkalmazott, célzott radioterápia.
Az újdonság nem csak a fehérje megismerésében van: 1996-ban a Nancy Carrasco által vezetett kutatócsoportnak sikerült a fehérjét kódoló gént visszafejteni, később pedig klónozni, és módosítani is tudták. Az áttörést az adja, hogy úgy tűnik, sikerül bejuttatni a működő NIS molekulát olyan daganatokba is, ahol nem fordul elő.
Kiderült, az is hogy a NIS nemcsak jodidiont képes pumpálni, hanem a sokkal jobban sugárzó, ezért erősebb terápiás hatást gyakorló perrenátot is. A molekula módosításával sikerült azt is elérni hogy a hatékonyabb perrenát radioizotópot sokkal jobban halmozó NIS-mutánst állítsanak elő, amely nagyobb hatékonysággal pusztítja el a daganatokat.
A kutatók felismerték, hogy amennyiben a NIS-t sikerül olyan daganatokba is bejuttatni, ahol természetszerűleg nincsenek jelen, akkor azok gyakorlatilag célzottan gyógyítható válnak.
Brachyterápia
A módszer az úgynevezett közel besugárzás, vagy brachyterápia típusba tartozik, a radioaktív forrást magába a daganat szövetbe próbálják behelyezni. Ilyen kezeléssel már 1901 óta próbálkoznak, száz éve még radioaktív tűket tűzdeltek a daganatba. A NIS radioaktívizotóp-pumpa génterápiás bejuttatása a daganatba mindezt célzott molekuláris módon teszi lehetővé.
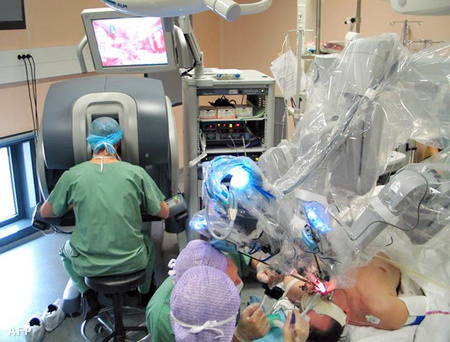
A közeli besugárzás hatalmas előnyökkel jár: szemben a többi módszerrel, minimális a sugárterhelés, az a nagyon gyengén jelenlévő, amely a kezelés végrehajtásából adódik, gyorsan kiürül a szervezetből. Ennél még nagyobb pozitívum, hogy ilyen esetekben nagyon alacsony a másodlagos daganat kialakulásának esélye. Ezzel szemben a sugárterápiák mellékhatásaként az egyik eltüntetése után nagyon gyakran újabb daganat alakul ki, sokszor teljesen más típusú, máshol. Előfordulhat, hogy szövődményként kialakult daganat agresszívebb, veszélyesebb, mint ami ellen eredetileg küzdöttek.
Pontosabb képet kaphatunk
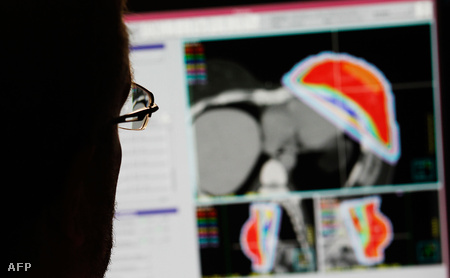
Az eljárás során használt radioaktív izotópok (radiojód, perrenát) segítségével lekövethetőek az emberi szervezetben lévő daganatok, olyan korszerű képalkotók alkalmazásával mint a SPECT-CT és a PET-CT.
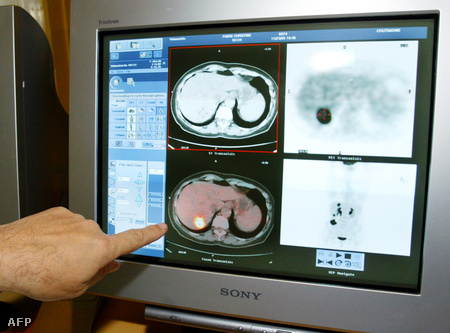
Ezeket a radioizotópokat már régóta alkalmaznak a gyógyításban, de az eddigiek kisebb pontossággal működtek, nagyobb volt a szórásuk, egészséges részeit is megjelölték a testnek. Tehát azzal, hogy célozhatóvá, ezáltal gyógyíthatóvá vállnak a daganatok, egyben könnyebben beazonosíthatóvá is.
Állatokon már működik
A kutatások jelenlegi állása szerint a módszert állatkísérletekben számos daganat (emlő, prosztata, melanóma, glióma) gyógyítására sikerrel alkalmazták. Emberben prosztatadaganat gyógyítására folynak már kísérleti vizsgálatok. A humán alkalmazásra még körülbelül tíz évet kell várni, hiszen az ilyen eljárások emberi szervezetre történő átültetése igen bonyolult feladat.
Bár technikailag minden rendelkezésre áll – a rendszer legdrágább technológiai része a SPECT-CT-t, amit itthon gyárt a 2010-ben Magyar Innovációs Nagydíjat kapott MEDISO –, Magyarországon még nincsenek önálló kutatások ebben a témában. Azt leszámítva persze, hogy Dohán egy ideje a New York-i csoporttal együttműködve itthonról publikál a külföldi szaklapokba. Ez remélhetőleg a közeljövőben megváltozik. Az eddig elért eredményeket Dohán Orsolya amúlt héten 29. alkalommal megrendezett Magyar Onkológus Társaság kongresszusán mutatta be a magyar szakmai közösségnek.