Gyilkos agysejtek megbékítése gyógyíthatja a Parkinson-kórt
További Tech-Tudomány cikkek
-
 Egy korszak vége: már a Disney+ sem tolerálja a jelszómegosztást
Egy korszak vége: már a Disney+ sem tolerálja a jelszómegosztást - Újra divat a döglött lazac fejdísz a kardszárnyú delfineknél
- Magyar kutatók megmérték az idegi jelek tulajdonságait
- Csaknem százmillió dollárt fizet az Apple a Siri miatt, mert az rögzítette a felhasználók beszélgetéseit
- Káprázatos csillaghullással kezdődik az év
A Parkinson-kór az Alzheimer után a második leggyakoribb neurodegeneratív (idegpusztulással járó) betegség. Ismert érintettek, mint például Michael J. Fox vagy Muhammad Ali sorsából tudható, hogy a betegség mozgásszervi rendellenességekkel, főként remegéssel jár, amit többek között az agy mozgatóműködésében fontos szerepet játszó substantia nigra (feketeállomány) nevű agyrész idegsejtjeinek elhalása okoz. Bár egyes kezelések javíthatják a beteg mozgáskoordinációját, máig nem áll rendelkezésre olyan gyógymód, amely a betegség hátterében húzódó folyamatokat érintené. Egy Magyarországra hazatért, korábban Németországban kutató magyar idegtudós, Szegő Éva legújabb eredményei azonban
az első működő Parkinson-gyógyszer lehetőségét is felvetik.
Védelem a sejtpusztulás ellen
A sejtek energiaellátásáért felelős sejtszervecske, a mitokondrium hajdan önálló baktérium volt, így nemcsak a sejthártya borítja, de benne megtalálható a baktériumokra jellemző gyűrű alakú DNS maradványa is. Külső membránjában ülnek olyan receptorfehérjék, amelyek a mitokondrium és a sejt többi része közötti kommunikációhoz elengedhetetlenek. Amikor ezekhez köt egy szabályozómolekula, az számos folyamatot indíthat be a mitokondriumok belül, ezzel változtatva meg működését. Ilyen receptormolekula a transzlokátor protein-18 (TSPO18) is, amelynek fő feladata, hogy a sejtplazmából bejuttatja a koleszterint és a koleszterolt a mitokondrium belsejébe.
Ott a koleszterinből úgynevezett neuroszteroidok jönnek létre, amelyek rendkívül fontosak a teljes idegrendszer egészséges működése szempontjából - például a Parkinson-kór folytán kialakuló neurodegeneráció ellensúlyozásában is. A neuroszteroidok akkor képződnek megfelelő gyorsasággal, ha a TSPO18 jól szuperál. Vagyis - elméletben - ha a transzlokátor fehérje működését támogatjuk valahogy, azzal lassíthatjuk a Parkinson-kórt. Szegő Éva, a Német Neurodegeneratív Betegségek Kutatóközpontja korábbi kutatójának és munkatársainak eredményei pedig arra mutatnak, hogy
ez az álom valósággá válhat.
A világ egyik vezető idegtudományi folyóiratában, a Journal of Neuroscience-ben most megjelent tanulmányban kimutatták, hogy létezik egy molekula, amely a transzlokátor protein serkentése révén nyújthat védelmet az idegsejtek tömeges elhalása ellen.
A történet egy véletlen felfedezéssel kezdődött: már korábban rájöttek, hogy a receptorhoz kapcsolódó egyik vegyület alkalmas arra, hogy a pozitronemissziós tomográf (PET) felvételein láthatóvá váljék az ideggyulladás, vagyis például a Parkinson-kór súlyosbodására utaló egyik legfontosabb tünet. Viszont nem sokkal később az is kiderült, hogy a TSPO18-hoz kötődő egy másik molekula (úgynevezett ligandum), túl a diagnosztikai felhasználáson, a terápiában is hasznos lehet. A molekula (amelynek nevét a gyógyszerek reklámozását illető törvények miatt nem írhatjuk le) a szorongás kezelésében bizonyult hatékonynak a klinikai teszteken.
Szimulált Parkinson-kór
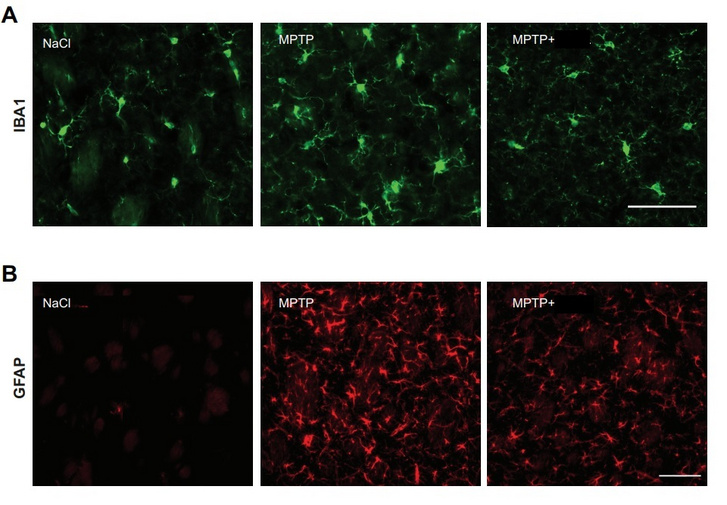
Tovább közelítve a Parkinson-kór felé, azt is felismerték az agykutatók, hogy ez a traszlokátor fehérje legnagyobb mennyiségben a mikrogliának nevezett agyi sejtekben jelenik meg. Ezek a sejtek leginkább az idegsejtek (neuronok) védelméért és a környezetük fenntartásáért felelősek, és ha gyulladás keletkezik az agyban, akkor a transzlokátor fehérjék még nagyobb számban jelennek meg a mikrogliákban. Minthogy tudott volt a kérdéses molekuláról, hogy köt a transzlokátor fehérjékhez, felmerült a kutatókban, hogy esetleg a mikrogliák működését is befolyásolhatja. Szegő Éváék többféle modellen (sejtkultúrákon és kísérleti egereken) is tesztelték a hipotézisüket.
Egereken gyakran szimulálják úgy a Parkinson-kórt, hogy egy MPTP nevű anyaggal kiirtják a substantia nigra dopaminerg (a dopamin nevű ingerületátvivő anyagra reagáló - M. Cs.) sejtjeit. Bár a hatásmechanizmusa nem teljesen egyezik a Parkinson-kóréval, az eredmény - például az ideggyulladás és a neuronok elhalása - ugyanaz. Az egerek egy részének az MPTP után adtunk ebből a gyógyszermolekulából is, és náluk az idegsejtek sokkal nagyobb arányban épek maradtak, mint a kontroll állatoknál.
- mondja Szegő Éva. A gyógyszerből annyit adtak az egereknek, ami testsúlyukhoz viszonyítva arányaiban megegyezett azzal a dózissal, amelyet a (szorongáscsökkentő célú) klinikai kísérletekben az emberek már bizonyítottan tolerálni képesek. Vagyis elméletileg ez a mennyiség a Parkinson-kór gyógyításában is biztonságos és hatékony lehet emberben is. A hatóanyag beadása után közvetlenül drasztikusan megváltozott a mikroglia sejtek génműködése, vagyis más fehérjék, más mennyiségben jelentek meg bennük. Középtávon pedig a gyulladás is, és az idegsejtek elhalása is jelentősen enyhébb volt a kezelt állatoknál.
Sőt, a sejtpusztulást majdnem teljesen meg is tudták állítani ezáltal.
Tehát a hatóanyag megvédi az idegsejteket, de nem képes visszahozni a halálból a már elpusztultakat, és pótolni sem tudja őket új neuronokkal. Noha néhány helyen, a korábbi közfelfogással ellentétben, felnőttkorban is képződnek új idegsejtek az agyban, a substantia nigra sajnos nem ilyen. Azok a sejtek, amelyek innen elvesznek, azok nem térnek vissza soha többé.
Rossz gyulladás
A neurodegeneratív betegségekben a gyulladások központi szerepet játszanak. Bár a gyulladás alapesetben az immunrendszer természetes reakciójának tekinthető, sokszor (mint például a Parkinson-kór esetében) kóros folyamattá válik, és segítség helyett éppenséggel fokozza a sejtpusztulást. Ezért terápiás cél lehet a gyulladás csökkentése. A túlságosan aktiválódott mikroglia sejtek maguk ölik meg a neuronokat, így a kutatók azt feltételezik, hogy ebbe az aktivációba tudtak a hatóanyag segítségével beavatkozni.
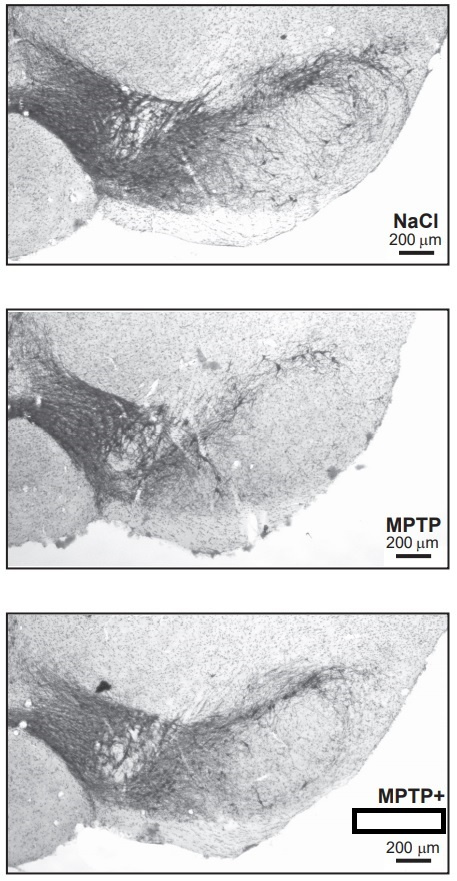
A mikroglia-aktiválás, leegyszerűsítve, két folyamatra bontható. Az első fázisban az idegsejtekre káros anyagokat termelő gliasejteket felváltják a neuronokat védő anyagokat termelő gliák. A gyógyszermolekula hatása az volt, hogy a mikrogliák sokkal hamarabb átmentek a káros fázisból a jótékony fázisba. Vagyis gyorsan rábírták a mikrogliákat, hogy a neuronok ölése helyett inkább azok védelmével és regenerálásával foglalkozzanak. De volt egy másik hatás is, folytatja Szegő Éva:
A molekula másik hatása nemcsak a mikrogliákban, de magukban az idegsejtekben is tetten érhető volt. Általános jelenség, hogy amikor az idegszövet pusztulásnak indul, a rosszul működő fehérjék eltakarítása lelassul a sejten belül. Ez stresszt, végül sejthalált okoz. A hatóanyag csökkenti e stresszt, és segíti, hogy a toxikussá vált fehérjeroncsokat a neuronok gyorsan kipucolják magukból.
Genetika és növényvédő szer
Amint látható, e módszer - ha egyszer emberi gyógyszer lesz belőle - sem a Parkinson-kór okát szünteti meg, hanem az eredményeként létrejövő rossz folyamatokat mérsékli. A siker szempontjából, azonban elsődleges jelentősége van az időnek. A tapasztalatok szerint, amikor egy emberről diagnosztizálják a Parkinson-kórt, a fontos idegsejtjeinek akár 60-80 százaléka már elveszett. Minél korábban kell felismerni a betegséget, hiszen csak a megmaradt idegsejtek megóvására van esély.
A hatóanyag további sorsa a Parkinson-kór gyógyításában egyelőre kiszámíthatatlan.
Ez nem originális molekula, már kapható a kereskedelmi forgalomban, így egy gyógyszercég szempontjából nem feltétlenül jelenthet nagy profitot a Parkinson-ellenes fejlesztése. Ugyanakkor állami támogatások segítségével el lehet érni, hogy idővel engedélyezetté váljon a klinikai gyakorlatban is. Jó hír, hogy mivel a szorongás ellenes felhasználása miatt a szükséges tesztek jó részén már átesett, vélhetően a kipróbálása a jövőben már egyszerűbb lehet. A Parkinson- kór és a vele rokon neurodegenerációs betegségek végső gyógyítása akkor kerülne kézzelfogható közelségbe, ha felfedeznénk kialakulásuk kiindulópontját. Ez azonban nem egyszerű.
Ha röviden kell válaszolni arra a kérdésre, hogy miért alakul ki a Parkinson-kór, akkor az az igazság, hogy nem tudjuk. Sejtések azért vannak. Az esetek körülbelül 10 százaléka egyértelműen genetikai eredetű. Vannak olyan génmutációk, amelyek egyértelműen a kór kialakulásához vezetnek, míg más mutációk növelik a betegség megjelenésének esélyét. De legalább ilyen fontosak a környezeti faktorok. A nehézfém- illetve egyes növényvédőszer-szennyezések is növelik a Parkinson-kór kockázatát
- érvel Szegő Éva. Igaz ez a légszennyezésre és az ivóvíz szennyezettségére is. Az élelmiszerekben található bizonyos rovarölőszer-maradványok is sokszorosára emelik a Parkinson-kór gyakoriságát. Nem csoda, hogy a laboratóriumi gyakorlatban a Parkinson-kór tüneteinek szimulálására használt hatóanyagok jó részét régebben használták a kémiai növényvédelemben is. Amikor e veszélyek még nem voltak ismertek, és a gazdálkodók mindenféle védelem nélkül lélegezték be a permetszereket, körükben jelentősen megnőtt a neurodegeneratív betegségek gyakorisága.
Bármi is okozza azonban a betegséget, jelenleg az elsődleges cél menteni, ami menthető.



