Így készül a koronavírus elleni vakcina

További Tech-Tudomány cikkek
Az új koronavírus ellen védő oltóanyagok fejlesztése és klinikai tesztelése soha nem látott tempóban fejlődik. Márciusban a kutatók csak óvatosan mertek fogalmazni: becslésekbe bocsátkoztak, legtöbbjük azt gondolta, másfél-két év is eltelhet, mire az első SARS-CoV-2 ellen védő oltás piacra kerül. Ma már jóval optimistább előrejelzések is vannak szerencsére, amire nagy szükség van: eddig harmincmillió koronavírusos megbetegedést regisztráltak, közel 920 ezer ember pedig belehalt a betegség szövődményeibe.
Jelenleg közel 150 értelmezhető vakcinaprojektet tartanak számon az egész világon, ebből nyolc a klinikai tesztek harmadik fázisában van már, mondhatni a véghajrában. Ez nagy örömhír, azonban az, hogy ténylegesen melyik lesz a sikeres oltóanyag, valamint az, hogy piacra kerülését követően a tömeges oltások mikor kezdődhetnek meg, sajnos nagyon bizonytalan. Számos tényező függvénye.
Hogyan készül a vakcina?
Egy speciális gyógyszer kifejlesztése rengeteg apró lépést, türelmet és hatalmas felelősséget rejt magában.
A VAKCINA GYÁRTÁSI FOLYAMATÁT ALAPVETŐEN KÉT NAGY FÁZISRA LEHET BONTANI. AZ ELSŐ A LABORATÓRIUMI, A MÁSODIK A KLINIKAI FÁZIS.
Kemenesi Gábor biológus, virológus, a Pécsi Tudományegyetem adjunktusa a Political Capital online kerekasztal-beszélgetésén elmondta:
Az első fázisban a kutatók többféle tesztet és kísérletet végeznek, sejteken és állatokon próbálják ki a lehetséges vakcinajelölteket.
Elmondása szerint több tervező laboratórium is részt vesz az átlátható oltóanyag fejlesztésében, ugyanis már az új koronavírus-járvány kitörése előtt is létrejöttek olyan szakmai szövetségek, amelyeknek egy esetleges vakcinatervezésnél a munkamegosztás és hatékonyságnövelés a célja. A precizitás és a gyorsaság a két fő szempont. „Ha laboratóriumi kísérletek igazolják, hogy egy vakcinajelölt hatásos lehet, megkezdődnek a klinikai vizsgálatok” – magyarázta a kutató.
Meddig tartanak a klinikai vizsgálatok?
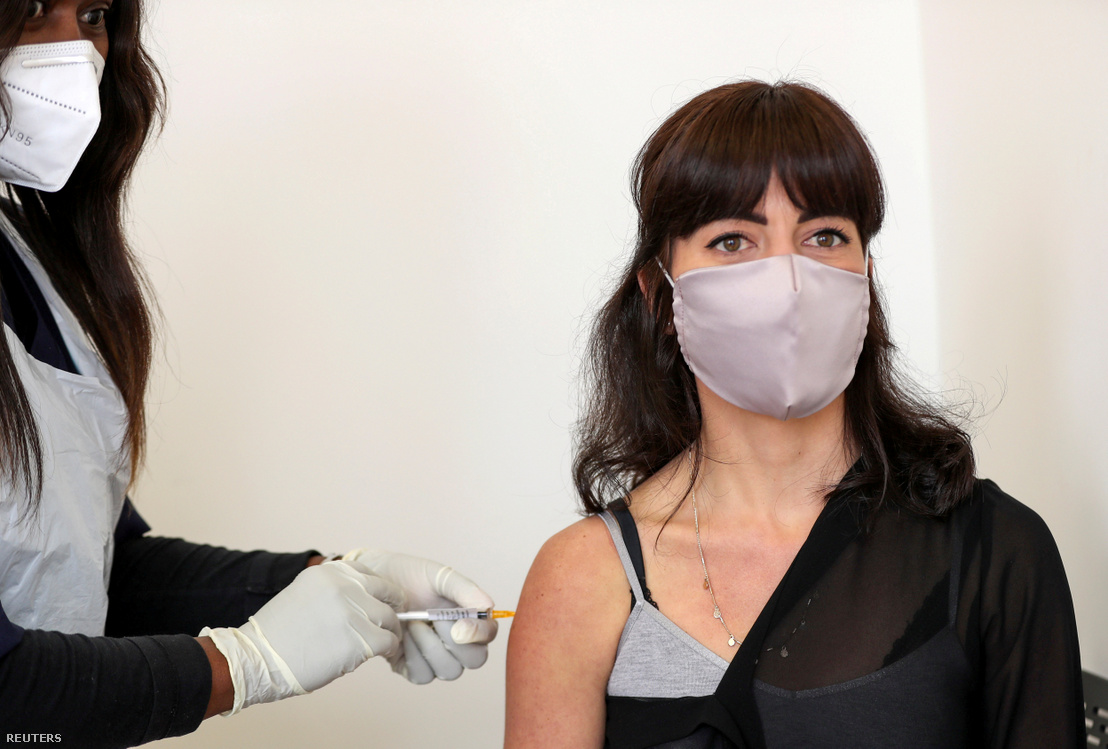
A klinikai vizsgálatok úgynevezett humán szakaszának négy egymás utáni lépcsője van.
- Először tesztelik, hogy az oltóanyag központi alkotóeleméből mekkora az emberi szervezetre vonatkoztatott megfelelő dózis, mennyit tolerál belőle, valamint felmérik azt is, hogy milyen immunválaszt vált ki. Biztonságos-e, okoz-e mellékhatásokat (ha igen, milyeneket), regisztrálják, hogy milyen gyorsan szívódik fel a véráramba és ürül ki a szervezetből.
- A második fázisban már egy kisebb csoport tagjain mérik fel, hogy a hatóanyag mekkora minimális dózis alkalmazásával hatásos, valamint ellenőrzik a válaszként keletkező immunreakció kémiai és biológiai tulajdonságait.
- Ha nem merül fel probléma a második fázisban, következik a harmadik lépés: a hatóanyagot több tízezer emberen kezdik tesztelni. Önkénteseket nagyon gyakran keresnek ilyen projektekhez. A beoltott emberek állapotát folyamatosan nyomon követik: vizsgálják, hogy a vakcina megvédi-e őket egy adott kórokozóval és betegséggel szemben, okoz-e olyan mellékhatást, amire laboratóriumi vizsgálatoknál nem derült fény. Ez a fázis emészti fel általában a legtöbb időt, ugyanis a hatásosságot egy új gyógyszer bevezetése után biztonsági előírásoknak megfelelően két évig figyelni kell.
- A negyedik, utolsó fázisban a hosszú távú hatásosságot és biztonságosságot nézik.
Lehet időt nyerni a klinikai tesztelés fázisában?
Mindezeket figyelembe véve nem csoda, hogy felmerül a kérdés: hogyan lehetséges, hogy 4-5 hónap alatt Covid–19 ellen védő vakcina kerüljön a patikákba? Azt sem igazán értik sokan, a gyártás és az engedélyezés időtartama hogyan lenne csökkenthető drasztikusan.
Ha a megfelelő anyagi és egyéb erőforrások rendelkezésre állnak, bizonyos fázisokon időt lehet spórolni. Mondjuk a klinikai tesztelés első két fázisa részben egymásba tolható, a harmadik pedig lerövidíthető: két év helyett hat hónapig vizsgálják a hatásosságot
– fejtette ki Kemenesi Gábor a Political Capital kerekasztal-beszélgetésén.
A klinikai fázisok lerövidítése, egymásba csúsztatása a virológus szerint nem veszélyezteti a biztonságosságot. „Ha egy oltóanyag a fejlesztés első két fent említett fázisában biztonságos, az azt jelenti, hogy az eredmény nyilvánosan elérhető tudományos publikációkban, független tudósok hivatkoztak rá.” Vagyis minden nyilvános.

Kemenesi Gábor szerint:
Egy másik út is járhatónak tűnik, de egyelőre még tárgyalási szakaszban van.
Ennek lényege, hogy beoltanak önkénteseket, majd nem várják meg, hogy lakókörnyezetben elkapják-e a koronavírust, hanem direkt megfertőzik őket vele. Az oltóanyag piacra kerülését azzal is jelentősen fel lehet gyorsítani, hogyha a gyártósorok, a betegtájékoztató és az árazás elkészül a klinikai tesztelés utolsó fázisára. Rizikója ennek is van, hisz egy esetleges hatástalanság, vagy mellékhatás ebben az esetben csak a piacra kerülést megelőzően derülne ki: ebben az esetben a fejlesztést az elejéről kell kezdeni.
Abban azonban minden szakember egyetért, hogy a hatások és mellékhatások, szakmai zsargonban a „biztonságosság″, az első.
(Borítókép: Laborítóriumi technikus kezeli az oltóanyag üvegeket, amelyekbe az Oxfordi Egyetem koronavírus vakcina jelöltjét az AZD1222 töltik, amelyet előkészítenek a nagy mennyiségű gyártásához és szállításához Anagniban 2020. szeptember 11-én. Fotó: Vincenzo Pinto / AFP)




