Most akkor halálos az emberi génszerkesztés, vagy nem?
További Tech-Tudomány cikkek
-
 Elégett egy aszteroida a Föld légkörében
Elégett egy aszteroida a Föld légkörében - Dán kutatók bizonyították: nem moderálják az önkárosító tartalmakat az Instagramon
- Azokkal a gázokkal mentenék meg a földet, amelyek miatt pusztulás fenyegeti
- Rengeteg új Nazca-vonalat talált a mesterséges intelligencia
- Senki sem fog örülni az Apple karácsonyi ajándékának, emelkedik egy népszerű szolgáltatás ára
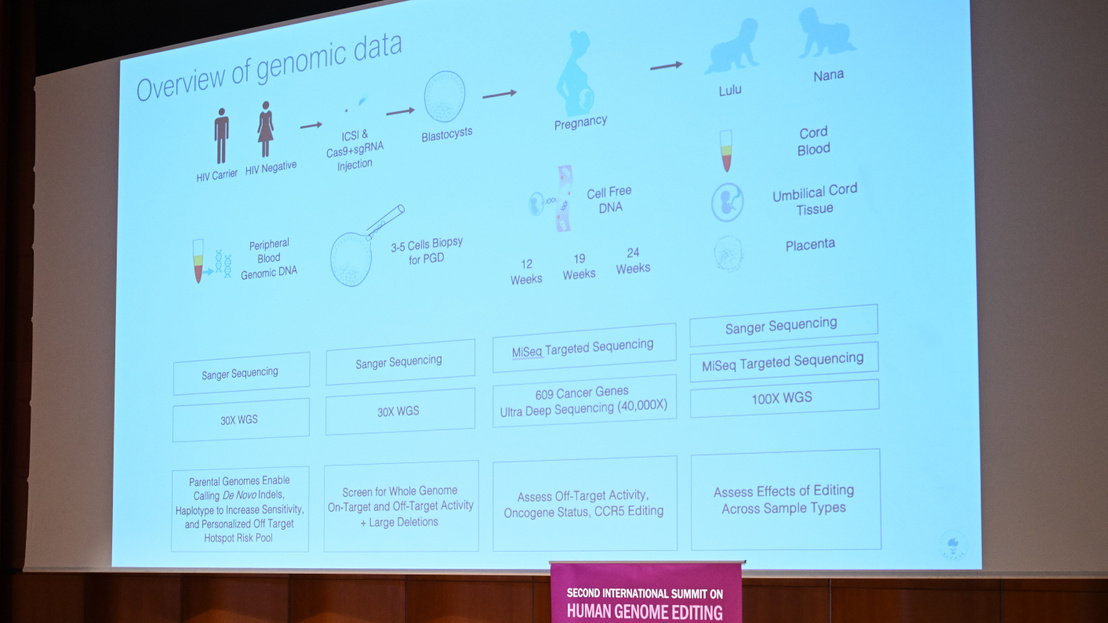
Júniusban jelent meg egy nagy visszhangot kiváltó tanulmány arról, hogy azok a személyek, akiknek genomjában két példányban van jelen a HIV elleni rezisztenciát okozó génváltozat, 21 százalékkal nagyobb valószínűséggel halnak meg 76 éves koruk előtt, mint a többségi populáció tagjai. Mindez azért kapcsolódik a génszerkesztéshez, mert a tavalyi, globális döbbenetet kiváltó emberkísérletben, amikor egy kínai genetikus két leánymagzat génjeit módosította, éppen ezt a gént akarta beültetni genomjukba. Vagyis elképzelhetőnek tűnt, hogy
ezzel éppen korai halálukat okozta.
Itt azonban az újabb fordulat: a cikk megjelenése után kapott, a kutatás módszertani hibáinak sokaságára rámutató kritikák hatására visszavonták a júniusi tanulmányt – ezzel szégyenkezésre késztetve nemcsak magukat, hanem a cikket publikáló Nature Medicine szaklapot is. Csakhogy megint vigyáznunk kell a következtetések hirtelen levonásával. Az, hogy a tanulmány nem bizonyította a génszerkesztés (pontosabban ennek az egy specifikus génnek a szerkesztése) veszélyes voltát, nem jelenti azt, hogy kimondhassuk: bizonyítottan biztonságos.
Pedig nem ártana ezt gyorsan eldönteni, hiszen a technikai akadályok elhárultával egyre-másra tűnnek fel a vállalkozó kedvű kutatók, akik már holnap szerkesztenék az emberi géneket, csak az engedélyre várnak (vagy nem várnak rá).
Korai halál
Az eredeti cikk szerzői – mindketten a berkeley-i Kaliforniai Egyetem kutatói, szóval nem valami noname helyről jöttek – több mint 410 ezer ember genetikai adatait elemezték, amelyekhez a brit UK Biobank projekt adatbázisából jutottak hozzá. Az adatbázisban olyan személyeket kerestek, amelyek két működésképtelen alléllel rendelkeztek a CCR5 génből.
Ez az a gén, amely HIV-rezisztenciát kölcsönöz a birtokosának.
Úgy találták, hogy – számukra is rejtélyes okból – azok, akik homozigóták erre a génváltozatra (vagyis anyjuktól és apjuktól is működésképtelen allélt örököltek), ötödével nagyobb eséllyel halnak meg 76 éves koruk előtt – vagyis az ő szóhasználatukkal „korán”. Arra nem volt elegendő adatuk, hogy a 76 évnél idősebb korban érződő hatást becsülni tudják.
A CCR5 gén akkor került a figyelem középpontjába, amikor Ho Csien-kuj (He Jiankui), a nem túl ismert senzeni Déli Műszaki és Természettudományos Egyetem biofizikusa ezt próbálta beültetni a gondjaira bízott magzatokba (egyébként nem teljes sikerrel, hiszen a létrehozott mutáció nem tökéletesen egyezik meg a természetben is előforduló változattal). A berkeley-i kutatók is ezért kezdték vizsgálni, hogy a gén egyébként hogyan befolyásolja a hordozóinak egészségi állapotát.

A CCR5 gén olyan fehérjét kódol, ami szükséges a HIV-nek ahhoz, hogy bejusson a gazdaszervezet sejtjeibe. Vagyis ha az allél működésképtelen fehérjét kódol, akkor ezzel a HIV jelentette probléma nem probléma többé. A kísérletben ezért kivágtak a génből egy kis részletet, ezzel a természetben is jelen lévő – és közismerten HIV-rezisztenciát okozó – mutációt utánoztak.
HIV nem, influenza, nyugat-nílusi láz igen
A beavatkozás nyilvánosságra kerülése után azonnal megjelentek azok az ellenvélemények, amelyek szerint nem volt túl okos dolog pont ezt a gént szerkeszteni (persze, úgy általában őrültség volt az egész), mert tudott az is, hogy ugyanez a génmutáció cserébe érzékenyebbé teszi hordozóját az influenzára, illetve a nyugat-nílusi lázat okozó vírus ellen.
A berkeley-i kutatóknak éppen volt egy algoritmusuk, amely a genom-adatbázisokban való kereséssel képes volt az egyes mutációk hatását becsülni az élettartamra, ezért úgy döntöttek, hogy ezen a génen próbálják ki a programot. Az eredményeiket (vagyis a mutáció korai halált okozó mivoltát) a Nature által akkor megkérdezett szakértők lelkesen kommentálták, és nem tartották meglepőnek.
Volt, aki az autoimmun betegségekkel való összefüggésben látta a hatás okát, bár azt is megjegyezték, hogy a hatás nem tűnik erősnek, és a kutatásnak megvannak a maga korlátai, így
óvatosan kell bánni a túlzottan elragadtatott konklúziókkal.
Ebben annyira igazuk volt, hogy a tanulmány alig pár hónapig létezett éles tudományos közleményként, aztán a szerzők kénytelenek voltak azt visszavonni. Tették ezt azért, mert a megjelenés óta a hitetlenkedő kollégáik sora vette komolyan szemügyre az általuk is elemzett UK Biobank adatbázist, és az ő eredményeik nagyon nem egyeztek az eredeti konklúziókkal. Vagyis nem találtak bizonyítékot arra, hogy a CCR5 gén kérdéses mutációja valóban lerövidítené az életet.
Algoritmusbaki
Nem szándékos csalásról van szó: az algoritmus működött rosszul. Hibásan azonosította a mutációkat, így nem azokat az érintetteket találta meg, akik valóban érintettek voltak. Rasmus Nielsen, az eredeti cikk egyik szerzője elmondta, hogy azért álltak elő az eredményekkel (a fejlemények fényében) túl korán, mert úgy érezték, felelősségük van abban, hogy az ismereteket a nyilvánosság elé tárják. Az eredeti szerzők egyébként az eredményeket megcáfoló egyik tanulmánynak is szerzői, vagyis úgymond magukat cáfolták meg.
A kétkedők gyakorlatilag a cikk publikálása utáni percben megjelentek. Sean Harrison, a Bristoli Egyetem genetikusa még aznap este lefuttatott egy elemzést a UK Biobank adatbázisán a CCR5 mutáció melletti génrészletre keresve (az egymás mellett lévő DNS-szakaszok szinte mindig együtt öröklődnek), de nem talált semmiféle összefüggést az élettartammal.
Harrison találata egyre több kutató figyelmét keltette fel, és a Harvard Egyetem orvosi karán is ránéztek az elemzésre – immár Nielsen bevonásával, aki végig rendkívül együttműködő volt, így senki sem vádolja szándékos svindlivel. Kiderült, hogy rossz volt az algoritmus. Egy harmadik vizsgálat pedig független (finn és izlandi) adatbázisokban nem talált semmiféle összefüggést.
A kutatók és a folyóirat nem tehetett mást, mint hogy visszavonták a tanulmányt a feltárt jelentős módszertani hiányosságokra hivatkozva.
Ugyanakkor a cáfolatban részt vevő kutatók is hangsúlyozzák, hogy ettől még simán lehet fontos szerepe a működőképes CCR5 génnek, így nagyon nem kéne génszerkesztéssel elrontani, miközben azt sem tudjuk pontosan, hogy mi a funkciója.
Újabb versenyzők
Ez persze nem tántorítja el azokat a kutatókat, akik szerint a génszerkesztés túl hasznos molekuláris biológiai eszköz ahhoz, hogy ne használjuk fel azonnal az emberi gyógyászatban. Azóta már HIV-fertőzött egérben, sőt HIV-pozitív felnőtt emberen is sikeresen alkalmazták a génszerkesztést, így akadályozták meg a vírus bejutását újabb sejtekbe.
Denisz Rebrikov, a moszkvai Kulakov Országos Orvostudományi Kutatóintézet génszerkesztési laboratóriumának vezetője júniusban jelentette be, hogy pont azt a CCR5 HIV-rezisztenciát okozó mutációt akarja beültetni, amit Ho Csien-kuj is próbált, vegyes sikerrel. Rebrikov legalább azelőtt tette ezt a bejelentést, hogy ténylegesen is végrehajtotta volna a beavatkozást, és megígérte, hogy erre csak az orosz hatóságok engedélye után kerülhet sor. Minthogy azóta nem sokat lehetett hallani erről a tervről, vélhetően elhalt valahol a dolog (ha volt valójában ilyen terv, és Rebrikov nem csak hírnevet akart magának szerezni az egésszel).
Az orosz genetikus azonban most újra hallatott magáról.
A téma megint csak magzatok génszerkesztése, de már nem a CCR5 gén a célpont, hanem egy örökletes siketséget okozó mutáció kijavítása. Az első hírek még arról szóltak, hogy a kutató már meg is kezdte a kísérleti beavatkozásokat olyan anyák által biztosított petesejteken, akik hordozzák a siketséget okozó gént. Később Rebrikov azzal pontosított, hogy nincs szó klinikai beavatkozásról, a vizsgálatokat a mutációt nem hordozó (halló) nőktől származó petesejteken végzik. A kutatómunka jelen szakaszának az a célja, hogy teszteljék, vajon a beavatkozás milyen nem kívánt mutációkat okoz a genomban.

A kérdéses, GJB2 jelű gént hordozó emberek hallása rossz, rendszerint hallókészülék nélkül nem képesek a mindennapokban előforduló hangokat megfelelő módon érzékelni. Ha valaki homozigóta a mutáns génre, az teljes siketséget okoz. Minthogy gyakoriak azok a párok, ahol mindkét fél homozigóta a mutáns génre, ők biztosak lehetnek benne, hogy gyermekük is siket lesz. Rebrikov állítása szerint már
több pár jelentkezett nála, akik alávetnék magukat (pontosan a születendő gyermekük kiinduló megtermékenyített petesejtjét) a beavatkozásnak.
Az orosz egészségügyi minisztérium a hírek hatására kiadott egy közleményt arról, hogy a génszerkesztett magzatok előállításának idejét még nem látja elérkezettnek, ebből arra lehet következtetni, hogy Rebrikov nem fogja egyhamar megkapni a várva várt engedélyét. Ebben egyetértenek az Egészségügyi Világszervezet (WHO) szakértői bizottságával, akik egyértelműen elítélnek minden efféle emberek végzett kísérletet:
Jelenleg bárki részéről felelőtlenség lenne génszerkesztést használni gyerekek létrehozására, mivel a DNS-ben bekövetkező változások átöröklődhetnek a következő nemzedékekre
– írtuk korábban. A bizottság ugyanakkor nem látta indokoltnak az összes ezt célzó laboratóriumi kutatás hatósági leállítását. Bejelentésüket megelőzően ugyanis egy nemzetközi kutatókból és szakemberekből álló csoport az emberi petesejtet, spermát vagy embriót érintő génszerkesztés ideiglenes betiltására szólított fel. A bizottság szerint nincs szükség ilyen szintű korlátozásra, ám hangsúlyozta, hogy a humán génszerkesztési kutatásokat kizárólag tudományos céllal, átlátható módon lenne szabad végezni.



