A herpeszvírus meghackeli az emberi sejtek kommunikációját
További Tech-Tudomány cikkek
-
 Ezzel a trükkel biztosan kiheverhető a szilveszteri másnaposság
Ezzel a trükkel biztosan kiheverhető a szilveszteri másnaposság - Egy ház árával vetekszik az LG új átlátszó tévéje
- Vékonyodik a középkategóriás mobilok piaca
- Különleges eljárást teszteltek Szegeden, ami sokak életét könnyítheti meg világszerte
- Több százezer magyar személyes adatait árulják a dark weben egy adatszivárgás miatt
Az ELKH Természettudományi Kutatóközpont (TTK) Biomolekuláris Kölcsönhatások Kutatócsoportja vezetésével magyar, amerikai és olasz kutatócsoportokból álló nemzetközi konzorcium vizsgálta, miként változtatja meg a gazdasejt osztódását szabályozó enzimek működését egy herpeszvírus-fehérje.
A kutatók a projekt keretében többek között felfedezték a sejtes jelátviteli folyamatok gyenge pontjait, és újabb lehetőségeket tártak fel a humán sejtek növekedési zavarainak visszaszorítása terén. A kutatás eredményeit bemutató tanulmány a Nature Communications folyóiratban jelent meg.
Kiismerték az embert
A Kaposi Mór által 1872-ben először leírt és róla elnevezett szarkómabetegségről a múlt század végén állapították meg, hogy kialakulása a herpeszvírus-fertőzéshez köthető. A herpeszvírusok olyan DNS-vírusok, amelyek már régóta az emberrel együtt fejlődnek, és egészséges emberekben ma már nem okoznak jelentős betegségeket. A kutatók éppen ezért feltételezték, hogy az ilyen vírusok alaposan kitanulták a gazdaszervezet működését, így azt a nekik megfelelő módon tudják módosítani, ezáltal megszelídült formában modellként alkalmazhatók.
A nemzetközi konzorcium biokémiai módszerekkel és számítógépes szimulációk segítségével tanulmányozta a Kaposi-szarkóma herpeszvírus (KSHV) egyik fehérjéjének (ORF45) hatását az emberi sejtekre. Megállapították, hogy a KSHV ORF45 fehérje a sejtnövekedésben fontos jelátviteli pályák két meghatározó fehérjekinázát egyszerre köti, ezáltal a gazdasejten belüli természetes komplexek kialakulásának és szétválásának dinamikája megváltozik, ami aztán megnövekedett sejtnövekedési jelpálya-aktivitáshoz vezet.
Mivel a kinázok olyan enzimek, amelyek más fehérjék működését foszforiláció – azaz egy gyakori kémiai fehérjemódosítási mechanizmus – révén változtatják meg, a vírusfehérje jelenlétében megnő a fehérjék egy csoportjának foszforilációja.
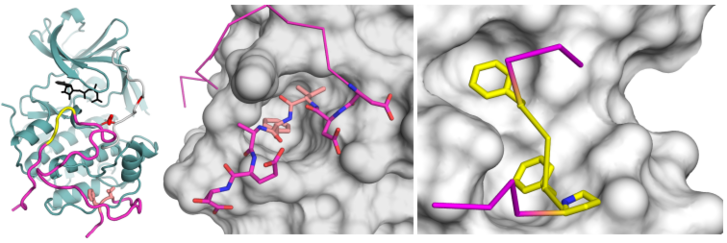
A kutatócsoport atomi felbontású felvételeket is készített a két enzim és az ezek kötésére szakosodott vírusfehérje-régiók által alkotott komplexekről. Az eredmények nemcsak arra adtak magyarázatot, hogy a vírusfehérje miképpen programozza át az emberi fehérjekomplexek működését, hanem a kutatók olyan ismeretlen fehérje-fehérje kölcsönhatásokat is feltártak, amelyek a gazdasejt megfelelő működéséhez is eleve szükségesek.
Átprogramoz ezt-azt
A herpeszvírus-fehérjék a molekuláris szintű zavarkeltés nagymesterei, ami a gazdasejtekben patológiás működéshez vezet. A Kaposi-szarkóma herpeszvírus – hasonlóan más vírusokhoz – kiismerte a sejten belüli bonyolult szabályzórendszerek gyenge pontjait. A konkrét mechanizmus molekuláris mimikrin, azaz utánzáson alapszik, amely során a vírusfehérje olyan fehérjefelszínekhez kötődik, amelyek a sejtnövekedés és sejthalál kényes egyensúlyának a beállításáért felelős enzimeken helyezkednek el.
A „szelíd vírusok” által alkalmazott biokémiai trükkök megismerése a humán sejtek növekedési zavarainak – például fokozott sejtosztódás, rák vagy fokozott sejthalál, gyulladás – visszaszorítására kínál újabb és újabb lehetőségeket. A kutatócsoport most olyan vegyületeket fejleszt, amelyek a sejtnövekedést manipuláló vírusfehérjék által is kedvelt fehérjékhez kötődnek.
(ELKH)




